EmendoBioのゲノム編集技術について【第4回】有害機能を獲得した遺伝子を確実に削除するためのゲノム編集戦略
第4回目は、有害機能を獲得した遺伝子を確実に削除するためのゲノム編集戦略について、説明します。
先回は、SNPを標的としたゲノム編集戦略について説明しましたが、DNAをSNPの部位で切断するだけでは、有害な遺伝子を確実に削除することはできません。
CRISPRヌクレアーゼを用いたゲノム編集では、ガイドRNAとヌクレアーゼの複合体が標的DNA配列を切断しますが、切断されたDNAは細胞が内在している修復機構によってつなぎ合わされます。この時、全く元通りに修復されると、その配列は再びゲノム編集の標的になりますが、切断・修復を繰り返すうち、修復の際に塩基の挿入や欠失が起きることがあり、結果的に元の配列と異なった配列となり、DNA配列の編集が成立します。このようにしてDNA配列が変化することによって、遺伝子が働かなくなることが期待できるのですが、どのように修復されるのかは制御できないので、修復のされ方によっては、さらに有害なタンパク質が作り出されてしまう可能性も否定できません。
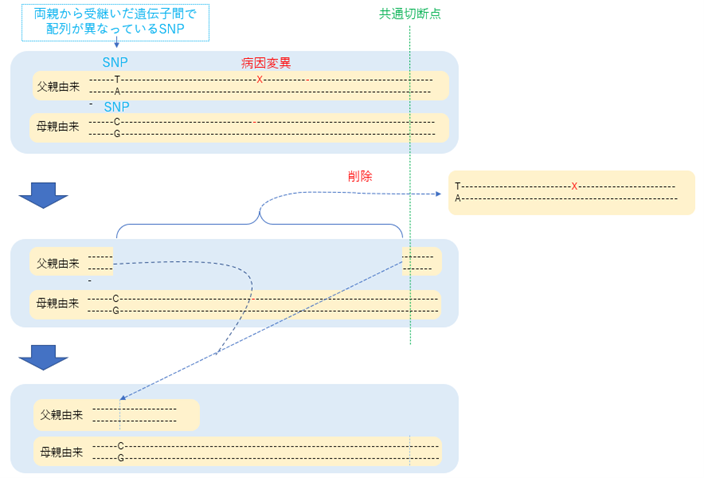
そこで、EmendoBioの編集戦略では、上記SNPの他にもう1ヶ所、アミノ酸配列を規定しない遺伝子配列(共通切断点)を選び、その箇所も標的として、2か所でDNAを切断し、病気の原因となる遺伝子のDNA配列の大部分を削除することによって、修復後に有害なタンパク質が出来てしまうリスクを排除しています。
継いだ2つの遺伝子のうち、病気の原因となる変異が存在する遺伝子上のSNPの配列を切断しますが、もう1ヶ所は、SNPではなく、2つの遺伝子とも同じ配列を持つ部位を切断します。この時、病気の原因となる変異をもつ遺伝子は2か所で切断され、切断された断片は削除されます。もう片方の正常な遺伝子は、SNPの配列では切断されませんが、もう1ヶ所は切断され、すぐに修復されます。修復の過程でDNA配列が変化することになりますが、この部分は、アミノ酸配列を規定していない部分なので、変化してもタンパク質の構造に影響を与えません。
実際に患者の造血幹細胞にこの方法でゲノム編集を施した結果について、第2回でご説明していますが、有害な機能を獲得して病気の原因となっている遺伝子が削除されると、もう片方の遺伝子の働きによって、造血幹細胞から好中球への分化・成熟する能力が回復していることが示されております。この時、異常のあるELANE遺伝子は削除され、同時に、正常なELANE遺伝子の方も、一旦切断され、切断部位のDNA配列が変化した状態でつなぎ合わされているはずですが、正常なELANE遺伝子は正しく機能していたことが解ります。
次回は、両親から受継いだ2つの遺伝子上のわずかな違いを区別できる精度の高いヌクレアーゼを作り出す仕組みについてご説明いたします。
